W Polsce w 2006 roku zéoéliwe nowotwory rozpoznane zostaná u ponad 120.000 chorych. Okoéo 1000 osû°b bádá to chorzy na szpiczaka mnogiego. ~1-2% wszystkich rozpoznawanych nowotworû°w to szpiczak mnogi (MM). Szpiczak mnogi jest drugá najczáéciej wystápujá cá na éwiecie chorobá nowotworowá ukéadu krwiotwû°rczego.
Terapia wspomagajá ca
- Zapobieganie nudnoéciom i wymiotom
- Terapia p-bû°lowa
- Leczenie zapalenia éluzû°wek jamy ustnej
- Pomoc psychologiczna
- Gorá czka neutropeniczna
- Leczenie anemii
- Zapobieganie i leczenie infekcji
- Polineuropatia
- Procesy zakrzepowo-zatorowe
- Lekarz i jego rola we wéaéciwym leczeniu
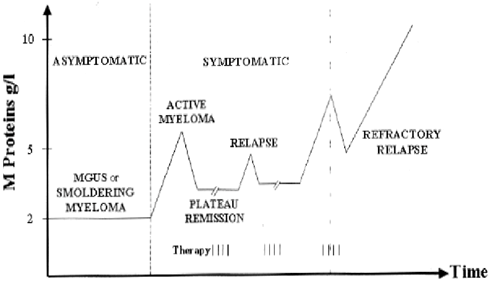
Naturalne fazy choroby
Typy infekcji oraz zapadalnoéá
- ã Ryzyko infekcji 7-15 x u chorych ze szpiczakiem mnogim (porû°wnujá c do innych hospitalizowanych pacjentû°w)
- Ryzyko infekcji jest niskie podczas fazy plateau, zaé wysokie podczas aktywnej fazy choroby
- Ukéad oddechowy ã czáste zapalenia péuc
- Ukéad moczowy ã ostre i przewlekée odmiedniczkowe zapalanie nerek
- Sepsa – posocznica
Infekcje zwiá zane z rû°é¥nymi stanami chorobowymi
- Faza poczá tkowa oraz nawrû°t -> infekcje wirusowe, grzybicze oraz bakteryjne
- Choroba w fazie stabilnej ã plateau -> géû°wnie infekcje Streptococcus pneumoniae lub Haemophilus influenze (oséabiona jest znacznie odpornoéá humoralna)
Czynniki predysponujá ce do infekcji
- Immunosupresja zwiá zana z chorobá (ã poziomu poliklonalnych immunoglobulin, ã aktywnoéci komû°rek NK, ã odpowiedzi B-komû°rkowej, ã proliferacji T-komû°rkowej na stymujacjá antygenowá )
- Neutropenia ã stan zwiá zany z leczeniem lub choroba zasadniczá
- Chemioterapia oraz leczenie sterydami
- Uszkodzenie éluzû°wek oraz skû°ry (cewniki, chemioterapia, radioterapia)
Czynniki infekcyjne
- Bakterie ã ziarenkowce (Pneumococci, Haemophilus influenze, Menigococci)
- Gronkowce ã infekcje zwiá zane z cewnikami centralnymi, portami oraz innymi cewnikami
- Bakterie Gram-ujemne (E. coli)
- Grzyby (Candida, Aspergillus)
Profilaktyka: roztwû°r doustny amfoterycyny B oraz Flukonazol w tabletkach - Wirusy (Herpes zoster, Herpes simplex, RSV, CMV)
Profilaktyka: Acyklovir, Valacyklovir, Foscarnet, Gancyclovir oraz inne leki - Pierwotniaki (Pneumocystis carinii)
Profilaktyka: Biseptol ã bardzo waé¥ne u chorych po procedurze przeszczepowej oraz leczonych dué¥ymi dawkami Dexametazonu
Infekcje wirusowe
RSV, Rhino-, Parainfuenza-, Influenza-, Adeno-, Corona-, CMV
Profilaktyka infekcji
- Szczepienia (Pneumococci, Haemophilus, Meningococci, Infuenza)
- G-CSF ã profilaktyka przy gorá czce neutropenicznej
- Doé¥ylne immunoglobuliny ã w dawce 0,4 g/kg mc co 3 tygodnie u chorych z czástymi infekcjami
- Antybiotyki (z grupy chinolonû°w, np. Palin, Abaktal, Cipronex)
- Penicyliny ã infekcje pneumo- i meningokokami
NALEé£Y UNIKAá AMINOGLIKOZYDûW - Leki p-wirusowe (Acyklovir, Gancyklovir, Foscarnet, Cidofovir i inne)
LECZENIE BARDZO WAé£NE U CHORYCH po PROCEDURACH PRZESZCZEPOWYCH oraz LECZONYCH DUé£YMI DAWKAMI STERYDûW (DEXAMETAZON)
Korzyéci péyná ce z ué¥ycia erytropoetyny
- Wzrost stáé¥enia Hb
- Redukcja iloéci przetoczonej krwi
- Zdecydowana poprawa jakoéci é¥ycia (apetyt, funkcje poznawcze, moé¥liwoéá áwiczeé fizycznych)
- Stáé¥enie Hb < 12 g/dl obserwujemy aé¥ u okoéo 70% chorych z multiple myeloma – ANEMIA
Leczenie wspomagajá ce
- Erytropoetyna (np. Aranesp, Neorecormon)
- Bisfosfoniany (np. Zometa, Aredia, Pamifos)
- Antybiotyki (np. klarytromycyna, chinolony)
- Leczenie p-bû°owe (plastry Durogesic)
- Czynniki wzrostu (G-CSF lub GM-CSF)
- Aparat ortodontyczny/gorset
- áwiczenia fizyczne
áwiczenia fizyczne (aerobowe) u chorych po procedurze auto-PBSCT
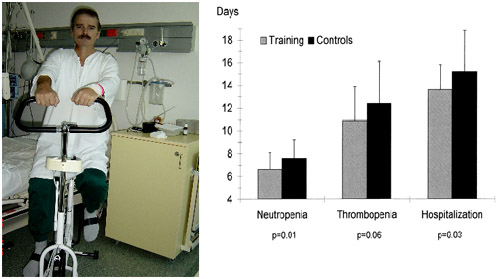
W wyniku systematycznych áwiczeé uzyskano ã czástoéci gorá
czek, ã leukopenii, ã nudnoéci i wymiotû°w, ã dobrego samopoczucia u pacjentû°w*
* Dimeo i wsp., Blood, 1997
Polineuropatia motoryczna po stosowaniu THALIDOMIDU ã czynniki ryzyka:
-
- Dawka kumulacyjna leku (< 20g: 10%)
- Wczeéniejsza terapia lekami neurotoksycznymi
- Polineuropatia istniejá ca przed rozpoczáciem terapii p-nowotworowej
- Wiek
- Niedobû°r witaminy B12 oraz kwasu foliowego istniejá cy u okoéo 20-30% osû°b z rozpoznaniem multiple myeloma
USZKODZENIE NERWûW W WYNIKU STOSOWANIA THALIDOMIDU JEST NAJCZáéCIEJ NIEODWRACALNE, W PRZECIWIEéSTWIE DO POLINEUROPATII PO TERAPII BORTEZOMIBEM.
Sposû°b postápowania w przypadku wystá pienia polineuropatii po leczeniu Thalidomidem i Bortezomibem
| Stopieé polineuropatii | Thalidomid | Bortezomib |
| Iô¯ bez bû°lu | Szczegû°éowe monitorowanie chorego | Szczegû°éowe monitorowanie chorego |
| Iô¯ z bû°lem lub IIô¯ | Redukcja dawki leku o 50% | Redukcja dawki do 1,0 g/môý |
| IIô¯ z bû°lem lub IIIô¯ | Zatrzymanie podawania leku, rozwaé¥enie podania Thalidomidu w mniejszej dawce | Zatrzymanie podawania leku, przy ustá pieniu objawû°w toksycznych podanie Bortezomibu 0,7 g/môý 1x w tygodniu |
| IVô¯ | Zatrzymanie podawania | Zatrzymanie podawania |
- Istotne jest uzupeénianie niedoborû°w wit. B12 oraz kwasu foliowego
- Rozwaé¥enie podania gabapentyny (Neurontin) po konsultacji neurologa
Zalety stosowania i aktywnoéá bisfosfonianû°w
- Efekt p-nowotworowy
- ã osteoklastogenezy
- ã IL-6
- ã apoptozy
- Efekt synergistyczny z Dexametazonem
- ã epizodû°w hiperkalcemii
- ã iloéci lekû°w p-bû°lowych
- ã czástoéci zéamaé kostnych
- Efekt p-bû°lowy
Rekomendacje – bisfosfoniany
| Lek | Kwas pamidronowy (np. Aredia, Pamifos, Pamitor) | Kwas zoledronowy (np. Zometa) | Kwas klodronowy (Clodronate) | Kwas ibandronowy (Ibandronate) |
| Dawka | 90 mg | 4 mg | 1600 mg | 6 mg |
| Czas infuzji | 3 godziny | 15 minut | 2 godziny | 1 godzina |
| Schemat podawania | 1x w miesiá cu | 1x w miesiá cu | 1x w miesiá cu | 1x w miesiá cu |
| Okres i czas podawania leku | Niezdefiniowany ã podawany nawet przy progresji choroby | Niezdefiniowany ã podawany nawet przy progresji choroby | Niezdefiniowany ã podawany nawet przy progresji choroby | Niezdefiniowany ã podawany nawet przy progresji choroby |
Osteonekroza szczáki po bisfosfonianach: ZOMETA i AREDIA
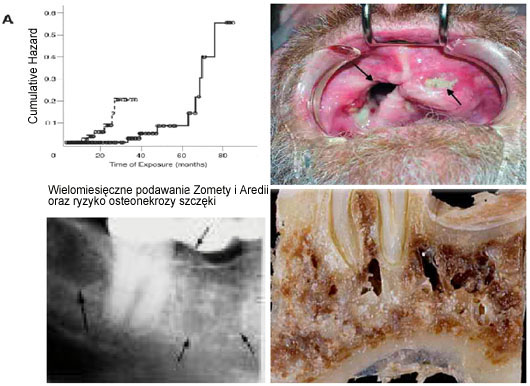
Rekomendacje zwiá zane z prewencjá /leczeniem osteonekrozy szczáki
- Badanie stomatologiczne zawsze przed wéá czeniem terapii bisfosfonianami
- Sanacja uzábienia jamy ustnej (higiena z wykorzystaniem géownie roztworu chlorhexydyny)
- Profilaktyka antybiotykowa przy wszelkich zabiegach stomatologicznych
- Zatrzymanie podawania bisfosfonianû°w przed i 2 miesiá ce po inwazyjnych zabiegach stomatologicznych
- Leczenie i zapobieganie zapaleniu éluzû°wki (mucositis)
Kyfoplastyka i vertebroplastyka – nowe sposoby terapii zalecane przez ortopedû°w
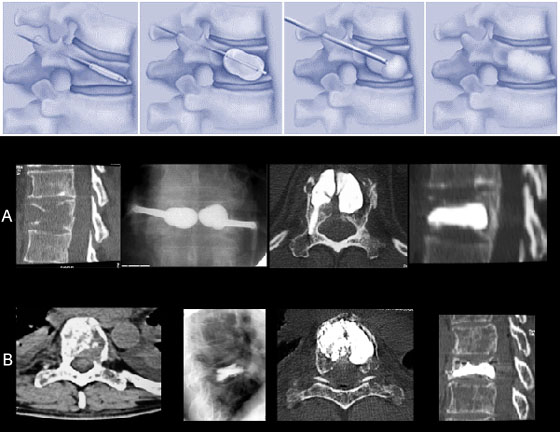
THALIDOMID jest zwiá zany z zakrzepicá é¥yé géábokich /DVT/
- Mechanizm powstania nieznany (Thalidomide powoduje: ã czynnikû°w prozakrzepowych, ã D-dimerû°w, ã czynnika VIII, powoduje aktywacjá péytek krwi oraz komû°rek endotelium)
- Ryzyko zdecydowanie roénie przy podawaniu dodatkowo sterydû°w (Dexametazon) oraz antracyklin (Doxorubicyna)
- Thalidomid powoduje géû°wnie DVT, bardzo rzadko dochodzi do zakrzepû°w tátniczych
Jaka jest przyszéoéá chorych na szpiczaka mnogiego w Polsce w 2006 roku?
- Naleé¥y zwiákszyá dostápnoéá do lekû°w, ktû°re powinny byá na staée ué¥ywane: THALIDOMIDE, REVLIMID, VELCADE oraz inne
- Powinno siá coraz bardziej wydéué¥aá remisje (faza plateau) oraz ulepszyá jakoéá é¥ycia chorych (quality of life)
- Naleé¥y zwiákszyá dostápnoéá do licznych randomizowanych badaé naukowych prowadzonych na caéym éwiecie
Chory z rozpoznaniem szpiczak mnogi powinien przede wszystkim:
- Dbaá o nerki (picie okoéo 3 litrû°w péynû°w, unikanie lekû°w nefrotoksycznych np. Ibuprofen, ué¥ywanie alternatywnych érodkû°w kontrastowych przy badaniu NMR lub CT)
- Unikaá infekcji (rodzina chorego oraz pacjent powinni siá regularnie szczepiá na grypá i inne choroby, naleé¥y myá ráce, banalna infekcja moé¥e spowodowaá sepsá)
- Wybraá sobie lekarza, ktû°ry jest zorientowany w optymalnym leczeniu choroby i jest na bieé¥á co odnoénie nowych sposobû°w terapii (waé¥na jest teé¥ wspû°épraca z nefrologiem, radioterapeutá , ortopedá oraz innymi specjalistami)
Terapia wspomagajá ca IDEALNY LEKARZ POWINIEN BYá*:
- Godny zaufania
- Empatyczny
- ãLudzkiã
- Cierpliwy
- Szczery
- Otwarty
- Peéen szacunku
- Sumienny
- Dokéadny
* Bendapudi NM Mayo Clin Proc, 2006
ô